Wróć
Wróć

Zespół jelita nadwrażliwego w chorobach o podłożu zapalnym. Wsparcie żywieniowe i probiotykoterapia
Zespół jelita nadwrażliwego a choroby zapalne jelit
Pacjenci chorujący na wrzodziejące zapalenie jelita grubego, oprócz objawów takich jak biegunka czy krwawienie z odbytu, skarzą się również na objawy żołądkowo-jelitowe, które mogą być podobne do objawów IBS. Dotyczy to szczególnie pacjentów w okresie remisji choroby podstawowej. Warto zwrócić uwagę na fakt, że etiologia zarówno wrzodziejącego zapalenia jelita grubego, jak i zespołu jelita nadwrażliwego pozostaje niejasna, jednak dla obu tych chorób wspólne są zaburzenia w składzie mikroflory jelitowej czy zaburzenia osi mózgowo-jelitowej. Nie bez znaczenia jest również to, że u pacjentów z wrzodziejącym zapaleniem jelita grubego w okresie remisji stwierdza się resztkowe zapalenia błony śluzowej jelita, co może predysponować do wystąpienia objawów IBS. Dysponujemy badaniami, które potwierdzają, że u pacjentów z UC w okresie remisji częstość występowania objawów zespołu jelita nadwrażliwego jest większa niż w przypadku osób zdrowych.
Postępowanie niefarmakologiczne w chorobach jelit
Duże znaczenie w terapii pacjentów z zespołem jelita nadwrażliwego ma odpowiednia dieta. Pierwszym etapem leczenia jest wprowadzenie zaleceń żywieniowych, które opierają się na regularnym spożywaniu posiłków o małej objętości – ok. 4–6 posiłków na dobę. Pacjent w trakcie spożywania posiłku powinien skupić się na dokładnym przeżuwaniu kęsów i spokojnym jedzeniu, co ułatwia trawienie. Kluczowe jest też nawodnienie organizmu.
Jeśli zmiana diety nie przyniesie oczekiwanych rezultatów i pacjent nadal odczuwa dyskomfort, należy rozważyć dietę eliminacyjną.
Dieta low FODMAP
Spożywanie fermentujących węglowodanów – takich jak oligosacharydy, disacharydy, monosacharydy oraz poliole – sprzyja nadmiernej fermentacji bakteryjnej i wzmożonemu wydzielaniu gazów, prowadząc do uporczywych wzdęć. Takie węglowodany mogą nasilać objawy IBS. Wprowadzenie diety ograniczającej ich spożycie istotnie statystycznie poprawia samopoczucie pacjentów z zespołem jelita nadwrażliwego. Co istotne, okres stosowania diety low FODMAP (low fermentable oligosaccharides, disaccharides, monosaccharides and polyols) nie powinien być dłuższy niż 4–6 tygodni. Wynika to z faktu, że dłuższe stosowanie takiej diety może spowodować znaczące zmiany w mikrobiocie jelitowej.
Wprowadzenie u pacjenta diety low FODMAP wymaga dużego doświadczenia i wiedzy. Pacjenci nie powinni na własną rękę stosować takich diet. Dieta ta wymaga od pacjenta dużej samokontroli i przestrzegania zaleceń. W pierwszym etapie całkowicie eliminuje się produkty zawierające fermentujące węglowodany. W tym czasie organizm nabiera tolerancji na te składniki, ale kluczowe jest konsekwentne przestrzeganie diety. W drugim etapie przeprowadza się tzw. test prowokacji, czyli stopniowo wprowadza się wyeliminowane na pierwszym etapie produkty. Istotna jest tu ścisła obserwacja organizmu, aby odkryć produkty, których organizm nie toleruje. Trzeci etap diety low FODMAP to ponowne wykluczenie produktów, które w fazie drugiej nadal powodowały u pacjenta dyskomfort czy uczucia wzdęcia.
Metaanalizy badań klinicznych wskazują, że zastosowanie diety low FODMAP w sposób istotny poprawia jakość życia pacjentów z IBS i łagodzi objawy choroby. Ze względu na trudności z odpowiednim jej zbilansowaniem dieta ta powinna być prowadzona przez doświadczonego dietetyka, aby u pacjenta nie wystąpiły niedobory pokarmowe. Wymaga ona również bardzo dużej samodyscypliny pacjenta w kwestii przestrzegania zaleceń.
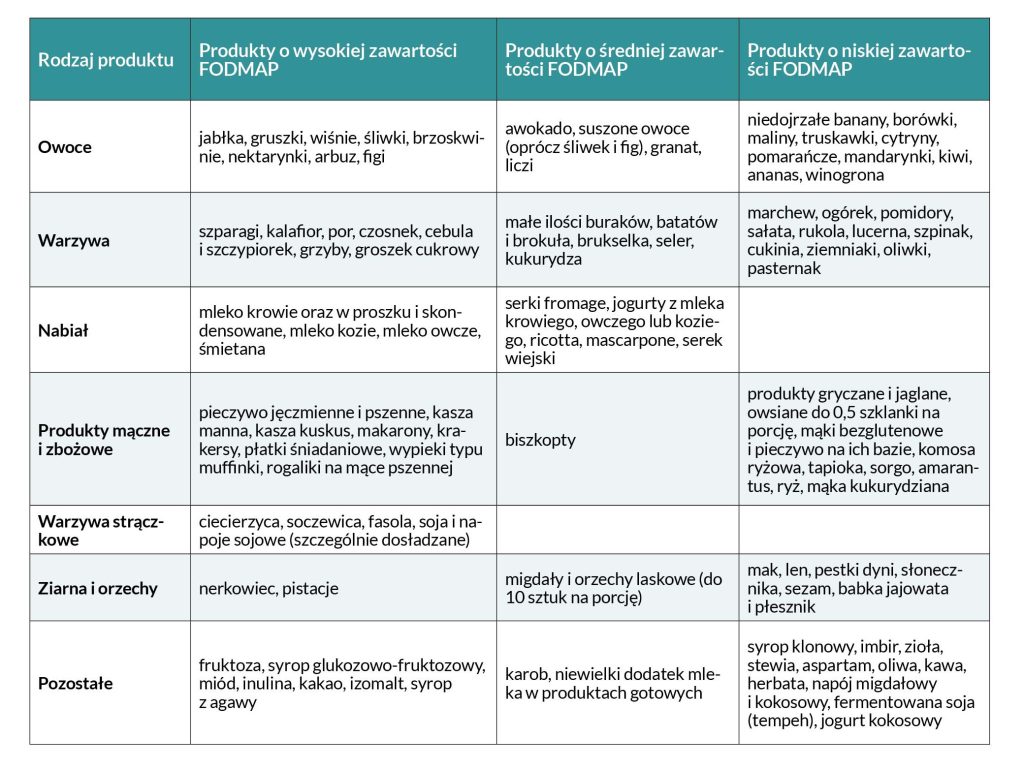
Produkty bogate w FODMAP oraz te dopuszczalne w diecie low FODMAP zawarto w tabeli poniżej.
Specyficzna dieta węglowodanowa
Gastroenterolog Sidney Hass w latach 50. ubiegłego wieku zaproponował inną dietę – tzw. specyficzną dietę węglowodanową (SCD – specific carbohydrate diet).
Polega ona na eliminacji węglowodanów złożonych – skrobi, laktozy, sacharozy – oraz produktów mlecznych. Ogranicza się również słodziki takie jak glukoza, maltilol, sorbitol, ksylitol, syrop z agawy, klonowy, daktylowy i melasę. Należy unikać również skrobi kukurydzianej, maltodekstryny, gumy guar czy karagenu.
W zależności od indywidualnej tolerancji pacjenta, ogranicza się także warzywa o wysokim potencjale fermentacyjnym, np. buraki, szparagi, brokuły, kalafior, kapustę, cebulę, czosnek i grzyby.
Ze względu na fakt, że dieta SCD, podobnie jak low FODMAP, jest dietą eliminacyjną, stosowanie jej wymaga konsultacji z doświadczonym dietetykiem. Istotne jest też, aby nie dopuścić do niedoborów wapnia na specyficznej diecie węglowodanowej – należy uzupełniać ten składnik np. napojami roślinnymi fortyfikowanymi w wapń.
Wpływ mikrobioty jelitowej na organizm
Rola i znaczenie prawidłowej mikrobioty jelitowej dla zachowania zdrowia – zarówno fizycznego, jak i psychicznego – to obiekt wielu badań naukowych. Ilość bakterii komensalnych występujących w układzie pokarmowym, oddechowym i moczowo-płciowym oraz tych bytujących na ciele około dziesięciokrotnie przewyższa liczbę komórek w naszym organizmie.
Warto wiedzieć, że istnieje szlak komunikacji między ośrodkowym układem nerwowym (OUN) a układem pokarmowym – nazywany jest osią mózgowo-jelitową. W prawidłowym funkcjonowaniu tej osi kluczowe znaczenie mają bakterie komensalne. Badania wykazały, że najistotniejsze dla dalszego zdrowia są pierwsze 2–3 lata po urodzeniu. Jeśli na początkowym etapie życie w jelitach nie będą skolonizowane pewne mikroorganizmy, w przyszłości może dojść do nadmiernej reakcji na stres oraz innych zaburzeń o charakterze psychicznym. Pacjenci chorujący na depresję czy zaburzenia lękowe w sytuacji stresu odczuwają nasilenie dolegliwości ze strony przewodu pokarmowego.
Połączenie to ma charakter dwukierunkowy – obecne są szlaki eferentne biegnące z OUN do jelit, odpowiadające za prawidłową perystaltykę czy ukrwienie, oraz szlaki biegnące z jelit do kory przedczołowej i układu limbicznego. Struktury te odpowiadają m.in. za przetwarzanie emocji, motywację, pamięć i samoświadomość.
Oprócz tego oś mózgowo-jelitowa związana jest z przekaźnictwem humoralnym – do krążenia ogólnego uwalniane są hormony, cytokiny, neuroprzekaźniki oraz metabolity bakteryjne.
Zalecenia ESPEN wskazują, że stosowanie kompleksu De Simone Formulation oraz bakterii z gatunku Lactobacillus reuteri w chorobach o łagodnym lub umiarkowanym nasileniu efektywnie indukuje remisję choroby.
Mikrobiota w chorobach jelit
W przypadku zespołu jelita nadwrażliwego zaburzenia równowagi mikrobioty jelitowej również wpływają na nasilenie objawów choroby. Jak wspomniano, pacjenci cierpiący na IBS mają zmniejszoną ilość tzw. dobrych bakterii z grupy Lactobacillus i Bifidobacterium. Zaobserwowano u nich z kolei przerost mikrobioty Escherichia coli, Streptococcus oraz Clostridium spp.
Przyczyną wystąpienia IBS może być przebyta infekcja przewodu pokarmowego (tzw. poinfekcyjny zespół jelita nadwrażliwego). Statystyki pokazują, że po 12 miesiącach od przebytej infekcji przewodu pokarmowego zespół jelita nadwrażliwego rozwinął się u prawie 15% pacjentów.
U pacjentów cierpiących na nieswoiste choroby zapalne jelit również zaobserwowano dysbiozę bakteryjną oraz zmniejszenie różnorodności flory bakteryjnej. Z tymi nieprawidłowościami związane są nieprawidłowości w komórkach błony śluzowej jelit oraz niekontrolowane reakcje układu odpornościowego.
Zastosowanie probiotykoterapii w przypadku pacjentów z zespołem jelita nadwrażliwego lub chorobami zapalnymi jelit może przynieść korzystne efekty – probiotyki poprawiają bowiem rytm wypróżnień i czas pasażu jelitowego. Wpływają na poprawę konsystencji stolca, a także zwiększają integralność błony śluzowej przewodu pokarmowego, chroniąc organizm przed wnikaniem czynników chorobotwórczych.
Prawidłowo dobrana probiotykoterapia może wspierać proces remisji stanu zapalnego jelit w chorobach typu wrzodziejące zapalenie jelita grubego.
Warto wspomnieć również, że jest to bezpieczna i praktycznie pozbawiona działań niepożądanych forma wsparcia konwencjonalnej terapii doustnej czy miejscowej.
Ogólne zasady probiotykoterapii
Probiotyk probiotykowi nierówny. Każdy ze szczepów bakteryjnych wymaga, aby przeprowadzone zostały badania w celu wykazania jego skuteczności oraz bezpieczeństwa stosowania. Nie należy ekstrapolować danych i wyciągać wniosków dotyczących skuteczności stosowania szczepu bakteryjnego, jeśli nie zostaną przeprowadzone takie testy.
Istotna jest również zastosowana dawka. Dla każdego szczepu bakteryjnego powinna zostać ustalona. Nie ma uniwersalnej, bezpiecznej i skutecznej liczby CFU (liczby jednostek tworzących kolonie – colony-forming unit), która pasuje do każdego szczepu bakterii.
Kluczowa jest też forma podania bakterii probiotycznych oraz ochrona ich przed np. niekorzystnym działaniem kwasu solnego w żołądku, tak aby bakterie miały możliwość skolonizować przewód pokarmowy.
Z tego względu najkorzystniej byłoby rekomendować wyłącznie preparaty probiotyczne o statusie produktu leczniczego. Niestety, na polskim rynku aptecznym jest ich zaledwie kilka. W zdecydowanej większości mamy do czynienia z suplementami diety, co do których powinniśmy zachować ostrożność w kwestii deklarowanej przez producenta zawartości szczepów bakteryjnych.
Przed zarekomendowaniem pacjentowi produktu probiotycznego warto upewnić się, że jego producent podaje konkretną i pełną nazwę szczepu – zgodną z obowiązująca nomenklaturą naukową – oraz deklarowaną zawartość wymienianych bakterii. Niedopuszczalne jest podawanie np. tylko nazwy samego rodzaju gatunku, np. Lactobacillus rhamnosus, bez podania pełnej nazwy szczepu.
Przypomnijmy, że pełna nazwa bakterii probiotycznej powinna składać się z trzech elementów – podania rodzaju (np. Lactobacillus), gatunku (np. rhamnosus) oraz szczepu (np. ATCC 53103).
Probiotykoterapia w IBS
Metaanalizy badań klinicznych oraz np. stanowisko WGO (World Gastroenterology Organisation) pokazują, że probiotyki mogą łagodzić objawy IBS i poprawiać komfort życia pacjenta. Należy jednak zastosować konkretne, przebadane szczepy bakterii.
I tak zastosowanie Bifidobacterium bifidum MIMBb75 u ponad połowy pacjentów z IBS przyczyniło się do poprawy komfortu życia.
Ponadto szczep Bacillus coagulans LBSC (DSM17664) okazał się skuteczny w przypadku IBS przebiegającego z biegunką, lecz również z zaparciami. Zmniejszał też wzdęcia, bóle brzucha, nudności czy uczucie przelewania się w brzuchu.
WGO rekomenduje także poniższe probiotyki:
- Lactobacillus plantarum 299v (DSM9843),
- Escherichia coli DSM17252,
- Lactobacillus rhamnosus NCIMB 30174,
- L. plantarum NCIMB 30173,
- L. acidophilus NCIMB 30175,
- Enterococcus faecium NCIMB 30176,
- Bifidobacterium animalis subsp. lactis BB-12®,
- L. acidophilus LA-5,
- L. delbrueckii subsp. bulgaricus LBY-27,
- Streptococcus thermophilus STY-31.
Ich stosowanie ma łagodzić bóle brzucha, objawy biegunki lub zaparć, a także zmniejszać wzdęcia.
De Simone Formulation
Wieloszczepowe preparaty probiotyczne są często rekomendowane przez ekspertów do łagodzenia objawów wielu chorób. Jedną z kompozycji stworzonych przez badaczy jest zestaw 8 szczepów probiotycznych określony jako De Simone Formulation. W jej skład wchodzą:
- Streptococcus thermophilus DSM24731,
- Bifidobacterium breve DSM24732,
- Bifidobacterium longum DSM24736,
- Bifidobacterium infantis DSM24737,
- Lactobacillus acidophilus DSM24735,
- Lactobacillus plantarum DSM24730,
- Lactobacillus paracasei DSM24733,
- Lactobacillus delbrueckii subsp. bulgaricus DSM24734.
De Simone Formulation ma udowodnione bezpieczeństwo zarówno w populacji osób dorosłych, jak i pediatrycznej. Probiotyki te wspierają efektywność terapii farmakologicznej.
Zalecenia ESPEN (European Society for Clinical Nutrition and Metabolism) wskazują, że stosowanie kompleksu De Simone Formulation oraz bakterii z gatunku Lactobacillus reuteri w chorobach o łagodnym lub umiarkowanym nasileniu efektywnie indukuje remisję choroby. Ponadto wymieniony kompleks probiotyczny wykazuje się lepszym efektem terapeutycznym niż stosowanie pojedynczych szczepów bakterii.
Źródła:
https://www.worldgastroenterology.org/UserFiles/file/guidelines/probiotics-and-prebiotics-english-2023.pdf, stan z dnia 22.05.2024.
Staniak N. Psychobiotyki w rekomendacji farmaceuty. Aptekarz Polski. Pismo Naczelnej Izby Aptekarskiej. 2018; 10: 10–23.
https://pubmed.ncbi.nlm.nih.gov/27623957/, stan z dnia 22.05.2024.
https://www.mp.pl/gastrologia/wytyczne/188516,choroby-czynnosciowe-jelit, stan z dnia 22.05.2024.
https://www.mp.pl/gastrologia/wytyczne/168224,probiotyki-aktualny-stan-wiedzy-i-zalecenia-dla-praktyki-klinicznej, stan z dnia 22.05.2024.
https://journals.viamedica.pl/forum_medycyny_rodzinnej/article/download/76045/63387, stan z dnia 22.05.2024.
https://food-forum.pl/artykul/czy-celowana-probiotykoterapia-moze-lagodzic-stan-zapalny-jelit, stan z dnia 22.05.2024.
https://food-forum.pl/artykul/ibs-w-nawrotach-o-podlozu-zapalnym-dieta-i-probiotykoterapia, stan z dnia 22.05.2024.