Wróć
Wróć

Nowe leki immunosupresyjne
Cyklosporyna to cykliczny polipeptyd złożony z 11 aminokwasów wytwarzany przez grzyb Tolypocladium inflatum. Jest silnym lekiem o działaniu immunosupresyjnym. Zapobiega odrzucaniu allogenicznych przeszczepów serca, nerek, wątroby, trzustki, jelita cienkiego, płuc i skóry; osłabia reakcję GvH („przeszczep przeciw gospodarzowi”) po przeszczepieniu szpiku. Hamuje humoralne i komórkowe reakcje immunologiczne, modyfikuje przewlekłe procesy zapalne, zmniejsza wytwarzanie i wydzielanie limfokin (m.in. IL-2), czynnika wzrostu komórek (TCGF), wpływa na limfocyty typu pomocniczego (Th). Hamuje fazę indukcji w procesie proliferacji komórek limfatycznych. Wskazania do stosowania cyklosporyny obejmują: zapobieganie odrzucaniu przeszczepu po allogenicznym przeszczepieniu narządów miąższowych, szpiku lub komórek macierzystych; leczenie odrzucania przeszczepu u pacjentów uprzednio otrzymujących inne leki immunosupresyjne; zapobieganie chorobie „przeszczep przeciw gospodarzowi” lub jej leczenie; czynne, zagrażające utratą wzroku zapalenie błony naczyniowej pośredniego lub tylnego odcinka oka pochodzenia niezakaźnego, gdy leczenie konwencjonalne jest nieskuteczne; steroidozależny i steroidooporny zespół nerczycowy u dorosłych i dzieci, wywołany przez choroby kłębuszków nerkowych, takie jak nefropatie z minimalnymi zmianami, ogniskowe i segmentowe stwardnienie kłębuszków lub błoniaste zapalenie kłębuszków nerkowych. Cyklosporyna może być także stosowana w celu wywołania remisji i jej utrzymania lub podtrzymania remisji wywołanej steroidami (możliwe wycofanie steroidów z leczenia). Ponadto, lek stosowany jest w leczeniu ciężkiego czynnego RZS, ciężkiej łuszczycy u pacjentów, u których konwencjonalne metody leczenia są nieskuteczne lub niewskazane oraz ciężkiego AZS wymagającego leczenia ogólnego.
Immunofiliny to białka odznaczające się zdolnością wiązania z substancjami immunosupresyjnymi. Uczestniczą w wielu procesach wewnątrzkomórkowych związanych m.in. z apoptozą, przesyłaniem sygnałów, przetwarzaniem RNA, stabilizacją kompleksów receptorów.
Leki działające na immunofiliny znalazły głównie zastosowanie w transplantologii, ale także chorobach skórnych, takich jak łuszczyca, atopowe zapalenie skóry, piodermia zgorzelinowa, rzadziej są stosowane w toczniu rumieniowatym. Do leków tych, poza cyklosporyną, zaliczają się takrolimus oraz sirolimus. Takrolimus poprzez wiązanie się ze specyficzną cytoplazmatyczną immunofiliną (FKPB-12) hamuje zależne od wapnia kaskady przenoszenia sygnałów w limfocytach T, zapobiegając w ten sposób transkrypcji i syntezie IL-2, IL-3, IL-4, IL-5 i innych cytokin, takich jak GM-CSF, TNF-α i IFN-γ. Sirolimus to wybiórczy lek immunosupresyjny hamujący aktywację limfocytów T indukowaną przez większość czynników pobudzających poprzez blokowanie wewnątrzkomórkowego przewodzenia sygnałów zależnego i niezależnego od jonów wapnia. Mechanizm działania polega na wiązaniu ze specyficznym białkiem cytozolowym FKPB-12, a powstający kompleks FKPB-12-sirolimus hamuje aktywację mTOR (mammalian target of rapamycin), co prowadzi do zablokowania wielu swoistych szlaków przewodzenia sygnałów w komórce. Powoduje to zahamowanie aktywacji limfocytów i odczynów immunologicznych, w tym także reakcji odrzucania przeszczepów. Ewerolimus jest lekiem o działaniu immunosupresyjnym oraz przeciwnowotworowym, który także polega na wiązaniu z białkiem FKBP-12. Ewerolimus jest inhibitorem sygnału proliferacji, wykazuje działanie immunosupresyjne przez hamowanie proliferacji i ekspansji klonalnej limfocytów T aktywowanych antygenem, poprzez interleukiny specyficzne dla limfocytów T, np. IL-2 i IL-15. Zahamowanie sygnału proliferacji prowadzi do zatrzymania komórek w fazie G1 cyklu komórkowego. Ewerolimus zmniejsza stężenie czynnika wzrostu śródbłonka naczyniowego, hamując proliferację komórek mięśni gładkich naczyń oraz angiogenezę guza. Ewerolimus jest silnym inhibitorem wzrostu i namnażania komórek guza, komórek śródbłonka, fibroblastów i komórek mięśni gładkich naczyń krwionośnych, hamuje glikolizę guzów litych in vitro i in vivo.
Mykofenolan mofetylu jest estrem 2-morfolinoetylowym kwasu mykofenolowego (MPA) o działaniu cytostatycznym na limfocyty T i B. Kwas mykofenolowy hamuje wybiórczo i odwracalnie dehydrogenazę monofosforanu inozyny, biorącą udział w syntezie nukleozydów guanozynowych niezbędnych do budowy DNA. Zmniejsza liczbę limfocytów i monocytów w ognisku zapalnym, nie zmniejsza aktywności neutrofili. Mykofenolan mofetylu stosowany jest w za- pobieganiu ostremu odrzucaniu przeszczepów narządów (nerka, serce, wątroba) w skojarzeniu z cyklosporyną i kortykosteroidami u biorców przeszczepów alogenicznych. Najczęściej występujące działania niepożąda- ne związane ze stosowaniem mykofenolanu mofetylu to: posocznica, kandydoza przewodu pokarmowego, zakażenie dróg moczowych, zakażenie wirusem opryszczki zwykłej, półpasiec, leukopenia, małopłytkowość, niedokrwistość, wymioty, ból brzucha, biegunka, nudności.
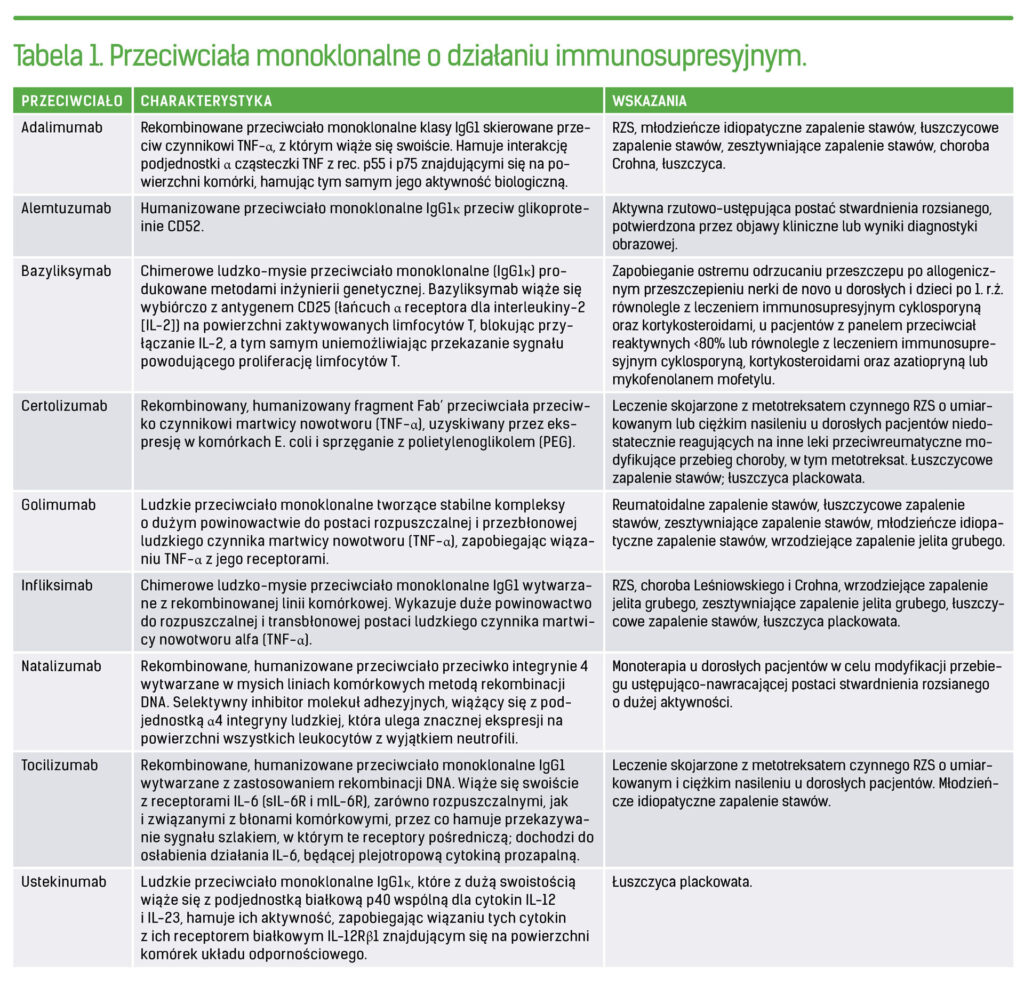
Przeciwciała znalazły szerokie zastosowanie w lecznictwie, zwłaszcza jako szybka i skuteczna metoda zapobiegania odrzucaniu przeszczepu. Biorąc pod uwagę ich swoistość, dzieli się je na mono- i poliklonalne. Przeciwciała monoklonalne (mAbs – monoclonal antibodies) to immunoglobuliny (IgG), które swoiście łączą się z innymi białkami (rozpoznają tylko jedną, ściśle określoną determinantę antygenową) obecnymi na powierzchni komórek znajdujących się w układzie krążenia lub w obrębie tkanek. Przeciwciała monoklonalne znalazły zastosowanie w różnych dziedzinach medycyny, w tym w onkologii, transplantologii oraz terapii chorób autoimmunologicznych. Należy zwrócić jednak uwagę na próby ich zastosowania w leczeniu innych chorób, takich jak: osteoporoza czy astma. Warto podkreślić ich zastosowanie w diagnostyce laboratoryjnej (podstawa testów diagnostycznych ELISA i RIA; m.in. w diagnostyce HIV); oczyszczaniu różnych substancji oraz w badaniach naukowych (m.in. selekcja i liczenie komórek (np. cytometria przepływowa), badanie różnorodnych białek komórkowych). W terapii przeciwnowotworowej przeciwciała monoklonalne mogą bezpośrednio wpływać (niszczyć) na komórki nowotworowe lub pośrednio wpływać na nie poprzez aktywację układu immunologicznego gospodarza. Mogą uruchomić odpowiedź immunologiczną w mechanizmie cytotoksyczności komórkowej zależnej od przeciwciał (ADCC) lub cytotoksyczności zależnej od dopełniacza (CDC). Komórki nowotworowe mogą również ulec zniszczeniu w wyniku indukowania przez przeciwciało apoptozy lub blokowania ekspresji zewnątrzkomórkowych białek istotnych fenotypowo. Przeciwciała monoklonalne mogą także blokować receptory komórkowe dla czynników wzrostu, w konsekwencji czego dochodzi do zahamowania wzrostu guza. Ponadto przeciwciała mogą działać na wybrane elementy mikrośrodowiska guza, na przykład na angiogenezę. Zastosowanie przeciwciał monoklonalnych o działaniu immunosupresyjnym przedstawiono w Tabeli 1. Preparaty o działaniu molekularnym, w tym przeciwciała monoklonalne, nie dają toksyczności charakterystycznych dla innych leków o działaniu immunosupresyjnym, jednakże są przyczyną innych niepożądanych objawów, także zagrażających życiu. Ponadto wciąż niewiele wiadomo o odległych skutkach leczenia molekularnego, ponieważ brakuje danych z długotrwałej obserwacji.
Bibliografia:
- Elżbieta Ograczyk, Magdalena Kowalewicz-Kulbat, Sebastian Wawrocki, Marek Fol. Immunosupresja – wymagający sprzymierzeniec na trudne czasy. Postępy Hig Med Dosw (online), 2015; 69: 1299-1312.
- W. Kostowski, Z. Herman. Farmakologia – podstawy farmakotera- pii, PZWL, 2006.
- https://indeks.mp.pl/desc.php?id=180, stan z dnia 14.12.2019.
- https://indeks.mp.pl/desc.php?id=1431, stan z dnia 14.12.2019.
- https://indeks.mp.pl/desc.php?id=955, stan z dnia 15.12.2019.
- https://indeks.mp.pl/leki/desc.php?id=7942, stan z dnia 15.12.2019.
Tekst opublikowany w numerze 1/2020 czasopisma Recepta