Wróć
Wróć
Pacjent pediatryczny z perspektywy farmaceuty
Ponadto, wchłanianie leków jest uzależnione od pH w żołądku. Tuż po urodzeniu ma ono wartość neutralną, w przeciągu 24–48 godzin spada do 3, po czym ponownie wzrasta do neutralnego i utrzymuje się na tym poziomie przez około 10 pierwszych dni życia. Dopiero około 2. roku życia pH w żołądku dziecka zbliża się do wartości jak u dorosłego. Z tego powodu niektóre leki, które są nietrwałe w środowisku kwasowym (np. penicyliny), mogą osiągać wyższe stężenia u noworodków niż u starszych dzieci. Natomiast leki o charakterze słabych zasad (np. itrakonazol) osiągają wyższe stężenia w niższym pH, a więc u noworodków stężenie leku będzie niższe.
Rozpuszczalność leków jest uzależniona także od wydzielania żółci. Przez pierwsze 3 tygodnie życia jej produkcja jest mniejsza niż u dorosłych, co powoduje różnice we wchłanianiu leków, zwłaszcza słabo rozpuszczalnych, np. hyrokortyzonu. Ponadto, u niemowląt procesy transportu przez błonę komórkową nie są w pełni wykształcone. Wyniki kilku badań oceniających wchłanianie leków sugerują, że dopiero około 4. m.ż. mechanizmy transportu biernego i aktywnego są w pełni wydajne. Kolejną istotną kwestią wpływającą na wchłanianie leków jest czas opróżniania żołądka i motoryka jelit. U noworodków i niemowląt czas opróżniania jest wydłużony, a motoryka obniżona, co przyczynia się do dłuższego przebywania leku w żołądku.
Wchłanianie przez skórę leków stosowanych miejscowo
Skóra u niemowląt i dzieci nie jest jeszcze w pełni wykształcona. Poszczególne warstwy skóry i naskórka są cieńsze i mniej zwarte. Między skórą właściwą a naskórkiem występują słabsze połączenia, a warstwa hydrolipidowa chroniąca naskórek przed działaniem czynników zewnętrznych i utratą wody nie jest dostatecznie rozwinięta. Poza tym, stosunek powierzchni skóry dziecka do jego wagi jest 2 do 3 razy większy niż u dorosłego.
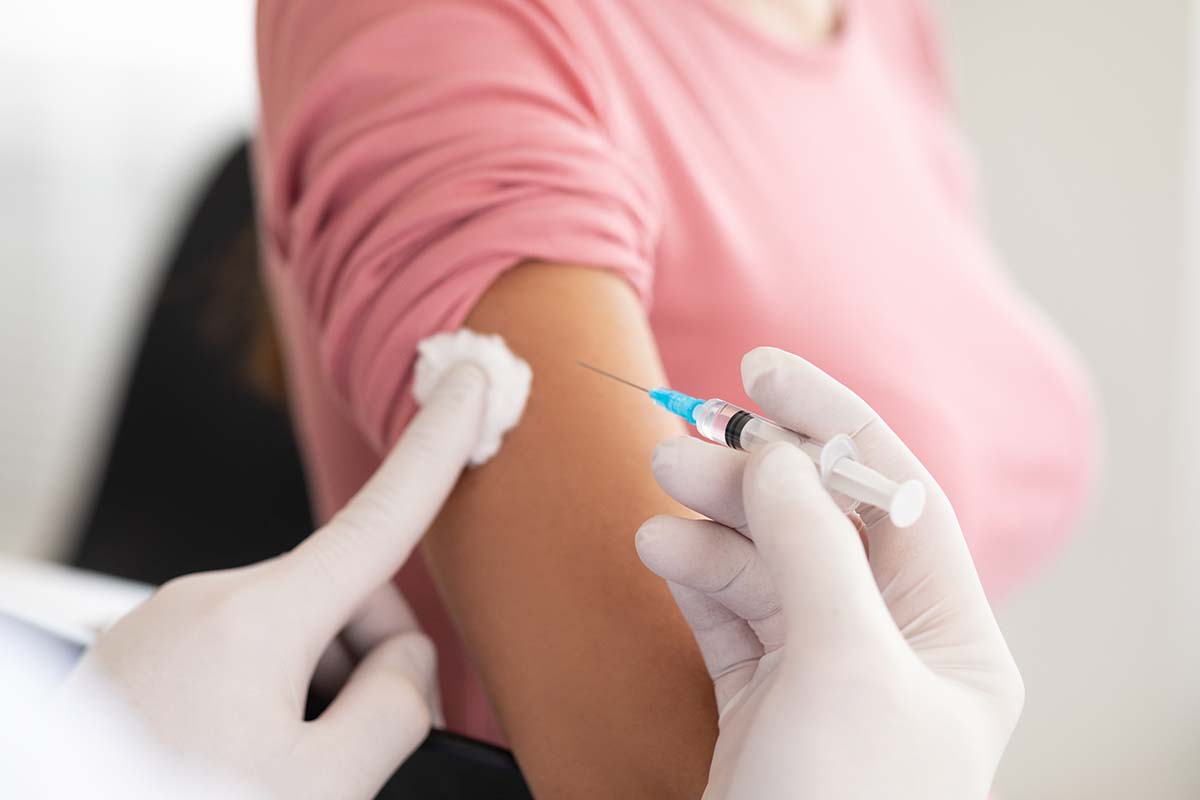
Wszystkie te czynniki przyczyniają się do łatwiejszego przenikania leków przez skórę dziecka. Dlatego też u niemowląt w przypadku preparatów do stosowania miejscowego z glikokortykosteroidami, aby uniknąć działania systemowego, zaleca się ich stosowanie przez maksymalnie 4–5 dni przy aplikacji raz dziennie. Natomiast ze względu na zwiększone wchłanianie przez skórę przeciwwskazane jest stosowanie leków zawierających kwas borny u dzieci poniżej 2. r.ż. ze względu na ryzyko kumulacji i zatrucia, które może prowadzić do niewydolności wątroby i nerek, a nawet zgonu.
U niemowląt szybkość eliminacji leku i ułamek jego wiązania z białkami osocza są zmniejszone, a biologiczny okres półtrwania jest wydłużony w stosunku do osób dorosłych, co wymaga zmiany dawkowania podawanych leków. W przeciwieństwie do noworodków i niemowląt, dzieci metabolizują wiele leków szybciej niż dorośli.
Dystrybucja
Dystrybucja zależy od właściwości chemicznych leku oraz od składu organizmu. W badaniu porównującym dane dotyczące farmakokinetyki 45 leków u dzieci i dorosłych zaobserwowano, że większa objętość dystrybucji częściej występuje u dzieci.
U noworodków około 80% objętości ciała to woda, a więc leki rozpuszczalne w wodzie powinny być u nich stosowane w większych dawkach na kilogram masy ciała niż u dorosłych. Dotyczy to np. morfiny, gentamycyny czy wankomycyny. Ponadto, leki lipofilowe mają stosunkowo większą objętość dystrybucji u niemowląt niż u starszych dzieci ze względu na różnice w zawartości tłuszczu (22,4% w 1. r.ż. w porównaniu z 13% w 15. r.ż.). Brak jest danych dotyczących dzieci otyłych.
Wpływ na objętość dystrybucji ma także stopień wiązania leku z białkami. U noworodków stężenie białek w osoczu wynosi 86% stężenia u dorosłych, a więc leki są w mniejszym stopniu wiązane z białkami. Udokumentowano to w przypadku stosowania m.in. fenytoiny, salicylanów czy penicylin. Można przyjąć, że dotyczy to wszystkich leków, które w dużym stopniu wiążą się z białkami.
Metabolizm
Metabolizm leków jest najbardziej złożonym etapem losów leku w organizmie i tutaj występują największe różnice między dorosłymi a dziećmi. Najbardziej dynamicznie zmiany przebiegają w pierwszych miesiącach życia i obejmują zarówno reakcje I fazy (m.in. utleniania, redukcji), jak i reakcje II fazy (reakcje sprzęgania, np. z kwasem glukuronowym).
Enzymy cytochromu P450 uaktywniają się już w życiu płodowym, ale ich aktywność zmienia się w kolejnych miesiącach ciąży i po narodzinach, osiągając poziom właściwy dla dorosłego około 2. roku życia. Podczas gdy większość enzymów zwiększa swoją aktywność w pierwszych miesiącach życia, niektóre ją tracą i zostają zastąpione innymi. W życiu płodowym główny izoenzym to CYP3A7, po urodzeniu jego aktywność zmniejsza się i pojawia się aktywność CYP2E1, CYP2D6, CYP3A4, CYP2C9 i CYP2C19. W trzecim miesiącu życia dziecka uwidacznia się aktywność izoenzymu CYP1A2. Najszybszy metabolizm wątrobowy wykazują dzieci w wieku szkolnym i młodzi dorośli – ma to związek z wysoką aktywnością izoenzymu CYP3A4, zwiększonym przepływem przez wątrobę oraz zwiększonym efektem I przejścia.
Kolejne różnice dotyczą reakcji II fazy. U dzieci w wieku 3–4 lat reakcja sprzęgania z kwasem glukuronowym nie jest w pełni wydajna, z związku z tym może u nich dojść do zaburzenia eliminacji m.in. paracetamolu, chloramfenikolu (tzw. zespół „szarego dziecka”) czy salicylanów. Z kolei reakcje metylacji, które u dorosłych praktycznie nie zachodzą, u noworodków i niemowląt przyczyniają się do przekształcania teofiliny do kofeiny.
Na metabolizm leków w przewodzie pokarmowym wpływa także mikrobiota jelitowa, której skład różni się w zależności od wieku. Poziom kolonizacji jelit przez bakterie osiąga u dzieci poziom jak u dorosłych mniej więcej około 4. roku życia. Jest to istotne w przypadku leków metabolizowanych także w świetle jelita, ponieważ wpływa na ich biodostępność i efekt farmakologiczny. Przykładem takiego leku jest digoksyna. Podejrzewa się, że na odmienny metabolizm digoksyny u dzieci wpływ ma aktywność enzymatyczna bakterii mikrobioty jelitowej. W związku z tym zaleca się zmniejszanie dawki digoksyny z wiekiem, tj. u niemowląt 45 μg/kg, u dzieci w wieku przedszkolnym do 35 μg/kg, natomiast u dzieci w wieku szkolnym 25 μg/kg.
Wydalanie
Wydalanie to ostatni etap losu leku w organizmie, który zależy głównie od efektywnej pracy nerek. Wartość współczynnika przesączania kłębuszkowego (ang. glomerular filtration rate, GFR) wzrasta w pierwszych miesiącach życia i osiąga wartość występującą u dorosłych do 1. roku życia dziecka. Ze względu na mniejszy GFR eliminacja takich leków jak antybiotyki aminoglikozydowe czy digoksyna jest mniejsza. Ponadto, wartość pH moczu u dzieci jest niższa, przez co może dochodzić do resorpcji zwrotnej leków o charakterze słabych kwasów.
U niemowląt szybkość eliminacji leku i ułamek jego wiązania z białkami osocza są zmniejszone, a biologiczny okres półtrwania jest wydłużony w stosunku do osób dorosłych, co wymaga zmiany dawkowania podawanych leków. W przeciwieństwie do noworodków i niemowląt, dzieci metabolizują wiele leków szybciej niż dorośli. Często należy im podawać wyższe dawki w mg/kg m.c., aby osiągnąć podobne stężenia leku w osoczu.
Postacie leków stosowane u dzieci
Postacie leków preferowane u dzieci to formy płynne, takie jak:
- krople doustne,
- roztwory,
- zawiesiny,
- syropy.
W przypadku niektórych substancji leczniczych (np. antybiotyków) ze względu na ich ograniczoną rozpuszczalność w wodzie uzyskanie trwałego roztworu stanowi problem, dlatego są one dostępne w postaci proszku, granulatu czy tabletek do sporządzania roztworu lub zawiesiny doustnej. Opiekun musi samodzielnie przygotować lek do podania dziecku, dlatego wydając tego typu preparat, udziel informacji na temat sposobu wykonania i przechowywania leku.
Małe dzieci nie potrafią połknąć tabletek, dlatego w przypadku stałych postaci leku dawki pediatryczne często występują w postaci:
- tabletek ulegających rozpadowi w jamie ustnej,
- pastylek do ssania,
- tabletek do rozgryzania i żucia.
Dostępne są także preparaty w postaci gum do żucia oraz lizaków. Gdy lek występuje w postaci tabletek powlekanych, a dziecko nie jest w stanie połknąć całej tabletki, w razie potrzeby opiekun może je rozkruszyć. Natomiast alternatywnym sposobem podania kapsułek, zawierających np. probiotyki, jest ich otwarcie i podanie dziecku samej zawartości. Informacje dotyczące możliwości dzielenia tabletek czy otwierania kapsułek zawarte są w ulotce.
Ponadto, ze względu na łatwość aplikacji małym dzieciom, często stosowane są również formy doodbytnicze – czopki i mikrowlewki. Zaletą podania doodbytniczego jest szybkie podanie leku i równie szybki efekt terapeutyczny.
Ważnym aspektem stosowania leków u dzieci jest tworzenie preparatów o akceptowalnym smaku i zapachu. Dlatego też w lekach pediatrycznych powszechny jest dodatek substancji poprawiających smak i zapach. Jeśli lek ma nieprzyjemny smak, istotną informacją dla opiekuna jest to, czy w razie konieczności można lek zmieszać z napojami lub pokarmem, które ten smak zamaskują. Jeżeli dziecko nie toleruje jakiegoś smaku, alternatywą może być wydanie odpowiednika z innym aromatem, np. Amoksiklav (400 mg + 57 mg)/5 ml zawiera aromat wiśniowy i cytrynowy, natomiast jego odpowiednik Augmentin MMF (400 mg + 57 mg)/5 ml – aromat pomarańczowy i malinowy.
Źródło:
Tuszyński, P.K. (red). Pediatria okiem farmaceuty. Tom I. Leki i problemy wieku dziecięcego, Wydawnictwo Farmaceutyczne, Kraków 2021.