
Zastosowanie leku recepturowego w terapii popromiennego zapalenia skóry. Cz. 3: Preparaty o działaniu przeciwbólowym i znieczulającym
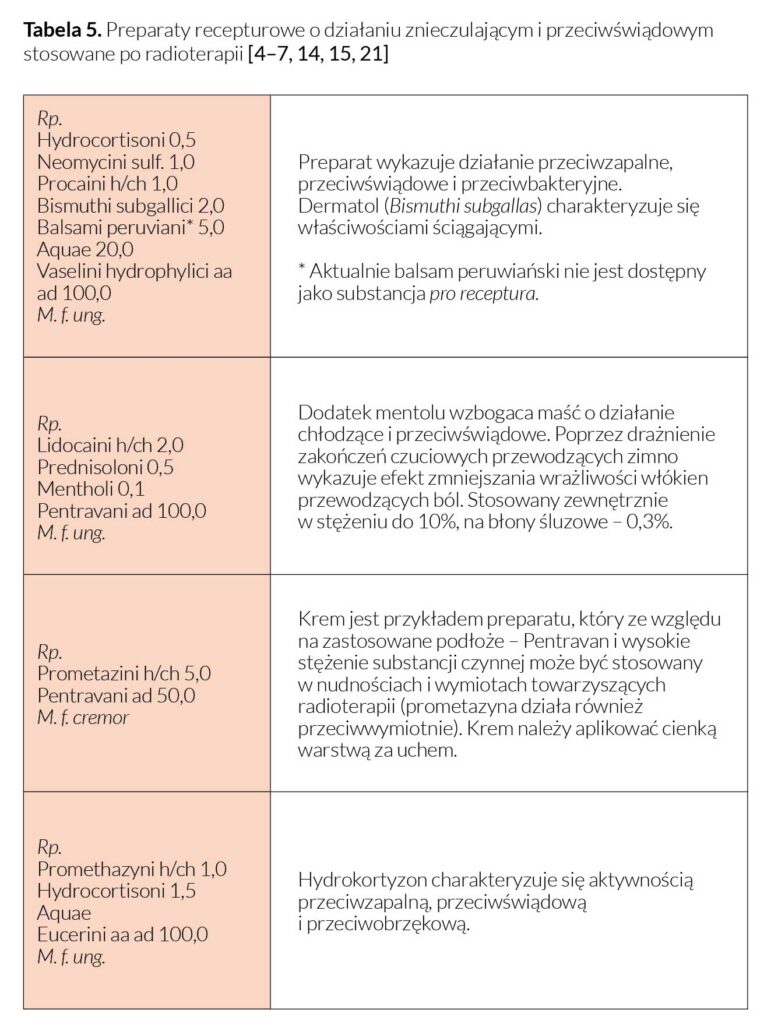
Promieniowanie powoduje również zwiększoną podatność na zakażenia, przede wszystkim grzybicze (pleśniawki) [1, 22]. W praktyce w przebiegu bolesnych stanów zapalnych w jamie ustnej stosowane są recepturowe płukanki, roztwory o zwiększonej lepkości do pędzlowania, układy dyspersyjne na bazie glicerolu czy zawiesiny z substancjami o działaniu przeciwbólowym, np. ketoprofenem, morfiną czy doksepiną, a także substancjami znieczulającymi i przeciwdrobnoustrojowymi [6, 7, 13, 23]. Doksepina należy do grupy trójcyklicznych leków przeciwdepresyjnych. Charakteryzuje się działaniem znieczulającym i przeciwbólowym, gdy stosowana jest zewnętrznie. Jej aktywność polega na tłumiącym działaniu na bodźce bólowe w skórnych nocyceptorach [23]. W Tabeli 6 przedstawiono przykłady preparatów do stosowania w jamie ustnej podczas radioterapii.
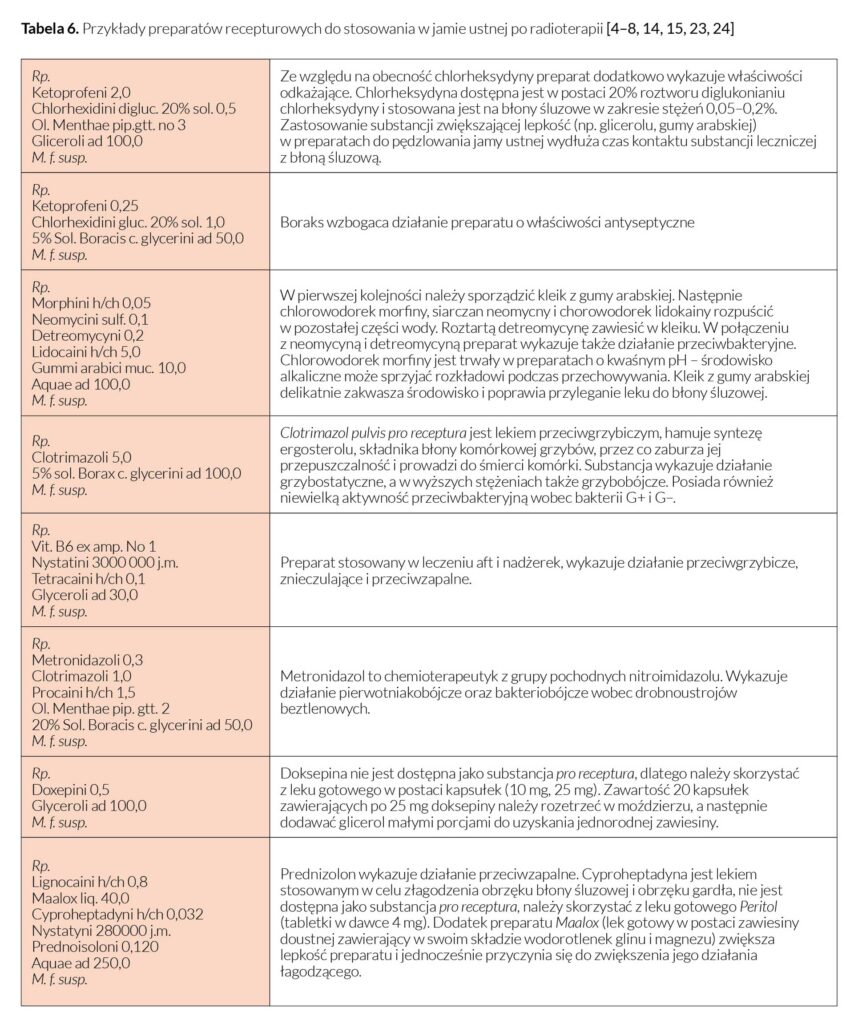
Objawem niepożądanym dotyczącym jamy ustnej jest również nadmierne wysychanie błon śluzowych w przebiegu radioterapii [1]. W celu łagodzenia suchości w jamie ustnej stosowany jest kwas winowy (wykaz B, FP XII). Jest to biały lub prawie biały krystaliczny proszek bądź bezbarwne kryształy. Bardzo łatwo rozpuszcza się w wodzie, łatwo w etanolu 96% [9]. Substancja stosowana jest u pacjentów z suchością jamy ustnej, wysuszeniem czerwieni wargowej, niedającym się opanować uczuciem stałego pragnienia. Poniżej przedstawiono przykład preparatu zawierającego w składzie kwas winowy. Do opakowania należy dołączyć sygnaturę „Zmieszać przed użyciem” [4, 5].
Rp.
Natrii citrici 3,0
Acidi tartarici 12,0
Glycerini 24,0
Ol. Menthae pip. gtt. 3
Aquae ad 250,0
M. f. mixt.
Źródła:
- Wiśniewski, M.; Graczyk, M.; Szpinda, M.; Mańkowska-Brzozowska, S. Popromienne zapalenie skóry – zasady postępowania. „Medycyna paliatywna w praktyce” 2013, 7, 41–46.
- Wolf, J.R.; Gewendter, J.S.; Bautista, J. et al. Utility of topical agents for radiation dermatitis and pain: a randomized clinical trial. SCC, 2020; 28: 3303–3311.
- Leczenie bólu wg Światowej Organizacji Zdrowia. Dostępne online: https://apps.who.int/iris/bitstream/handle/10665/43944/9241561009_eng.pdf (stan z dnia: 14.09.2021).
- Strona internetowa: akademiafagronu.pl (stan z dnia: 14.09.2021).
- Poradnik receptury współczesnej Fagron cz. 1, wydanie II poprawione. Fagron sp. z o.o. Kraków 2015.
- Pandyra-Kowalska, B. Receptura okiem praktyka – część czwarta. Recepturowe możliwości leczenia bólu. „Aptekarz Polski”. 15.05.2020.
- Jachowicz, R. (red.). Receptura apteczna. Sporządzanie leków jałowych i niejałowych. Wydawnictwo Lekarskie PZWL, Warszawa 2020.
- Wykaz surowców farmaceutycznych dopuszczonych do obrotu w Polsce. Dostępne online: https://sf.rejestrymedyczne.csioz.gov.pl/?AspxAutoDetectCookieSupport=1#results (stan z dnia: 14.09.2021).
- Farmakopea Polska XII. Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, Polskie Towarzystwo Farmaceutyczne, Warszawa 2020.
- Szymańska, E., Winnicka, K.: Euceryna eucerynie nierówna, „Bez Recepty”, 2014; 12: 24–27.
- Hylands-White, N.; Duarte, R.V.; Raphael J.H. An overwiec of treatment approaches of chronic pain management. Rheumatol. Int. 2017; 37: 29–42.
- Wiśniewski, M.; Szpinda, M.; Krakowiak-Sarnowska, E. Zastosowanie żelu z morfiną w leczeniu bolesnego owrzodzenia nowotworowego. Opis przypadku. Pol. Med. Paliatywna 2002; 1: 89–91.
- Bastami, S.; Frodin, T.; Ahlner, J.; Uppugunduri S. Topical morphine gel in the treatment of painful leg ulcers, a double-blind, placebo-controlled clinical trial: a pilot study. Int. Wound J. 2012; 9: 419–427.
- Gajewska, M.; Sznitowska, M. (red.). Podstawy receptury aptecznej. Materiały do ćwiczeń dla studentów farmacji. Fundacja Pro Pharmacia Futura, Warszawa 2019.
- Marszałł, L. Receptura apteczna półstałych postaci leków do stosowania na skórę w teorii i praktyce. Farmapress, Warszawa 2015.
- Ketoprofen, charakterystyka produktu. Dostępne online: https://www.mp.pl/pacjent/leki/leki/doctor_subst.html?id=444 3 (stan z dnia: 14.09.2021).
- Komatsu, T.; Sakurada, T. Comparison of the efficacy and skin permeability of topical NSAID preparations used in Europe. Eur. J. Pharm. Sci. 2012; 47: 890–895.
- Berardi, R.; Piga, A.; Pulita, F. et al. Effective prevention of 5-fluorouracil-induced phlebitis by ketoprofen lysinate salt gel. Am. J. Med. 2003; 115: 415–417.
- Makuła, M.; Szkutnik-Fiedler, D. Środki znieczulające miejscowo. Local anaesthetics. Farmacja Współczesna, 2018; 11: 83–88.
- Cantisani, C.; Ricci, S.; Grieco, T. et al. Topical promethazine side effects: our experience and review of the literature. Biomed. Res. Int. 2013; 151–509.
- Bourdon, F.; Lecoeur, M.; Leconte, L. et al. Evaluation of Pentravan®, Pentravan® Plus, Phytobase®, Lipovan® and Pluronic Lecithin Organogel for the trandermal administration of antiemetic drugs to treat chemotherapy-induced nausea and vomiting AT the hospital. Int. J. Pharm. 2016; 515: 774–787.
- Maria, O.M.; Eliopoulos, N.; Muanza, T. Radiation-induced oral mucositis. Front. Oncol. 2017; 7: 89.
- Jayakrishnan, R.; Chang, K; Ugurluer, G. et al. Doxepin for radiation therapy-induced mucositis pain in the treatment of oral cancers. Oncol. Rev. 2015; 9: 290.
- Varnadyan, R. Piperidin-4-ylidene substituted tricyclic compounds [w:] Piperidine-based drug discovery. Elsevier, 2017.







